消化器腫瘍内科
消化器腫瘍内科
消化器腫瘍内科の業務
1.消化器領域の腫瘍内科医の役割
消化器領域における悪性疾患は、食道・胃・小腸・大腸がん、胆道・膵臓がん、GIST、原発不明がん等の診断と薬物療法を中心とした治療を行っています。
治療方針の決定にあたっては、診療科内でのカンファレンスの他、キャンサーボードにおいて、外科・放射線科・病理など他科スタッフとの連携を密にして、
最適な治療を提供できる体制を整えています。消化器癌の診断、治療方針の決定、薬物療法を中心とした治療と、有害事象の管理、支持療法の実践を一貫して行います。
このため、病院全体の患者サポート部門である外来化学療法センター や
緩和ケアセンター
や
緩和ケアセンター において、当グループは主要な役割を果たしています。
またがんゲノム医療推進センター
において、当グループは主要な役割を果たしています。
またがんゲノム医療推進センター と協力して、
多くの方に遺伝子パネル検査を実施し、遺伝子異常に基づいた治療法を提供致します。
と協力して、
多くの方に遺伝子パネル検査を実施し、遺伝子異常に基づいた治療法を提供致します。
腫瘍内科というと、デスクワークが多い印象をもたれる方も多いと思います。しかし、消化器がんに関しては、内視鏡診断、内視鏡を用いた薬物療法の効果判定の他、消化管出血に対する内視鏡処置、
消化管閉塞・閉塞性黄疸に対するステント留置術など、緊急処置が多い事も特徴です。これらの緊急の処置もグループで対応する事を基本としています。
2. 新規の治療法開発への取り組み
新規治療の開発や現在の治療の問題点を明らかにするため、日本臨床腫瘍研究グループ(JCOG 肝胆膵グループ)、西日本がん研究機構(WJOG消化器グループ)、
北海道消化器癌化学療法研究会(HGCSG)などに所属しており、各がん腫における臨床試験や治験治療に積極的に参画しています。これらの体制を維持し、
常に最新の医療を実践していくために、がん薬物療法専門医の取得はもちろん、High volume centerへの留学、国内外の学会発表や論文作成、基礎研究等を通し、
常に知識と技術を蓄積していく事を目指しています。
(2024/05月)
食道/胃/大腸がんの薬物療法
以下に当施設での食道がん、胃がん、大腸がんの治療方針と臨床試験を示します。 いずれもガイドラインや臨床試験の結果に則り、最適な治療を致します。現在のエビデンスで補い得ない領域については、臨床試験や治験治療により対応しています。
1. 食道がん

2. 胃がん

3. 大腸がん

登録中の多施設共同前向き研究
食道がん
- 進行頸部食道扁平上皮癌患者に対してDocetaxel/Cisplatin/5-FU (DCF)と強度変調放射線治療(Intensity Modulated Radiation Therapy: IMRT)を同時併用する根治的化学放射線療法の第Ⅱ相試験
- 通過障害を有する食道癌に対するチェックポイント阻害剤併用薬物療法に関する多施設共同前向き観察研究
胃がん
- 進行・再発HER2陽性胃がん患者を対象とした三次治療におけるトラスツズマブ/デルクステカンの有効性の評価、及び一次治療後のバイオマーカーを探索的に検討する多施設共同前向きコホート研究(EN-MARK)
- 70歳以上 HER2陽性の治癒切除不能な進行・再発胃癌患者を対象としたトラスツズマブ/デルクステカンの多機関共同観察研究(EN-COURAGE study)
- 高度腹水を伴うまたは経口摂取不能の腹膜転移を有する胃癌に対するmFOLFOX6+ニボルマブ療法の第II 相試験(WJOG16322G)
- 切除不能進行再発胃腺癌もしくは食道胃接合部腺癌に対する3 次治療以降のFTD/TPI+RAM併用療法とFTD/TPI 単剤療法のランダム化第II 相比較試験(WJOG15822G)
- 切除不能進行・再発胃癌に対するニボルマブ再投与における有効性と安全性の前向き観察研究
大腸癌
- 切除不能大腸癌に対するトリフルリジン・チピラシル+ベバシズマブの従来法と隔週法の実用的ランダム化第Ⅲ相試験(PRABITAS)
- 根治的外科治療可能の結腸・直腸癌を対象としたレジストリ研究 (GALAXY trial)
- 血液循環腫瘍 DNA 陰性の高リスク Stage II 及び低リスク Stage III 結腸癌治癒切除例に対する術後補助化学療法としてのCAPOX療法と手術単独を比較するランダム化第 III 相比較試験 (VEGA trial)
(2024/05月)
胆道・膵臓がんの薬物療法
当院には、 が開設され、
同センタースタッフを主体とした肝胆膵キャンサーボードで議論された上で治療方針が決定されています。
が開設され、
同センタースタッフを主体とした肝胆膵キャンサーボードで議論された上で治療方針が決定されています。
また、国内を代表するの臨床研究グループである、日本臨床腫瘍研究グループ(JCOG)の肝胆膵グループのメンバーとして新規治療開発に積極的に参画しています。
胆道がんに対しては、長らくゲムシタビン+シスプラチンが標準治療とされてきました。しかし、2022年にチェックポイント阻害剤の有効性が報告され、本邦でも使用可能となりました。 また、フチバチニブ融合遺伝子陽性の 切除不能な胆道がんに対しては、フチバチニブの保険承認も得られました。有効性が高い治療を行うことにより、切除不能と判断された方でも、 根治切除が可能となる場合があり、薬物療法の効果を実感しています。
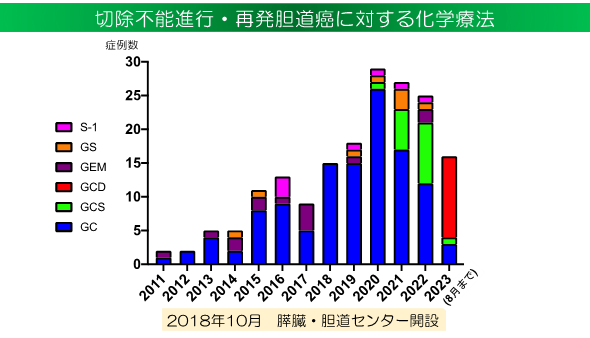
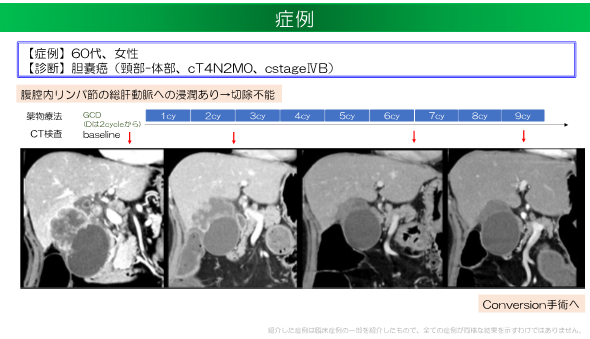
図: 本症例は当院の一部であり、すべての症例が同様な結果を示すわけではありません。
登録中の多施設共同前向き研究
- JCOG1901:消化管・膵原発の切除不能進行・再発神経内分泌腫瘍に対するエベロリムス単剤療法とエベロリムス+ランレオチド併用療法のランダム化第III相試験(JCOG1901)
- 切除不能または再発胆道癌を対象としたゲムシタビン/シスプラチン/S-1(GCS)療法と ゲムシタビン/シスプラチン/免疫チェックポイント阻害薬療法のランダム化比較第 III 相試験
(2024/05月)
遺伝性消化器腫瘍に対する診療
がんは遺伝子異常の蓄積により起こる疾患です。がんの治療に際して、遺伝子検査が多数行われるようになった事により、実は遺伝性のがんの疑いがある、といった事例がが多く認められるようになりました。
消化器領域では、リンチ症候群(大腸癌)、家族性大腸腺腫症、家族性膵癌等が代表的です。御本人やご家族に対しては、
遺伝子診療部 と協力して、
週1回の消化器遺伝外来を行っています。また、2023年より京都大学を中心に運営されている遺伝性腫瘍診療カンファレンスにコア施設として参加し、多施設での症例検討を行っています。
と協力して、
週1回の消化器遺伝外来を行っています。また、2023年より京都大学を中心に運営されている遺伝性腫瘍診療カンファレンスにコア施設として参加し、多施設での症例検討を行っています。

登録中の多施設共同前向き研究
- 家族性膵癌家系または遺伝性腫瘍症候群に対する早期膵癌発見を目指したサーベイランス方法の確立に関する試験
(2024/05月)
支持療法について
支持療法とは、癌に伴う症状や治療による副作用を軽減する目的で行われる予防策や治療を指します。最近の消化器癌の薬物療法は、多剤を併用する治療強度の強い薬物療法ですので、
適切に支持療法を行うこと必須と言えます。
薬物療法の副作用は、代表的なものとして、吐き気や便秘、倦怠感、口内炎、下痢などの消化器症状が挙げられます。また、分子標的薬剤の副作用には、血栓塞栓症や消化管穿孔があり、
免疫チェックポイント阻害剤の副作用の中には、腸炎や肝機能障害などが知られており、これらの管理には消化器内科医、ひいては内科医としての、幅広い知識や経験が求められています。
また、これらの副作用にどう対応するのか、という観点からの臨床研究は極めて少ない現状であり、これらの臨床研究に積極的に参画しています。更に、毒性はなぜ起こるのか、
といった発症機序も明らかにされていない点が多く、副作用の発症に関する基礎的研究にも、患者さんの唾液や糞便など検体を用いた菌叢解析の視点から取り組んでいます。
登録中の多施設共同前向き研究
- 進行期胃/大腸/膵/非小細胞肺がん患者に対するアナモレリン塩酸塩の効果予測因子に関する多施設共同後ろ向き観察研究
- 口腔内細菌叢とフッ化ピリミジン系抗がん剤による口腔粘膜炎のリスク研究
基礎研究について
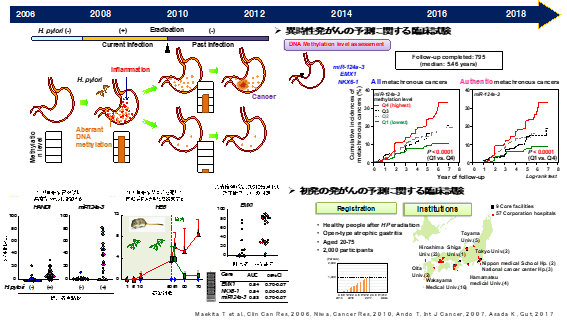
1. がん及び非がん部におけるエピジェネティック異常
様々ながん及び非がん部におけるエピジェネティックな異常を解析し、その意義を検討してきました。現在、H.pylori除菌後の胃粘膜に蓄積したDNAメチル化異常の量を測定し、 これが将来の発がんのマーカーとなり得るかを評価する臨床試験に参画しています。
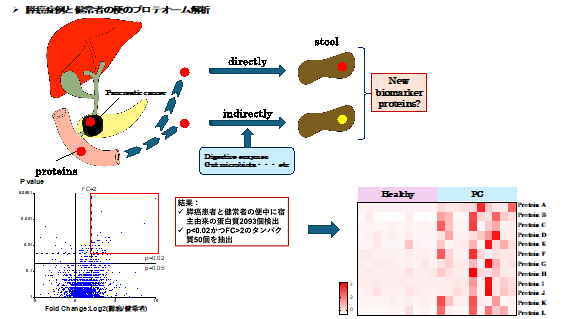
2. 膵がんの診断における便中のタンパクの同定
膵癌症例と健常者から便を回収し、プロテオーム解析を行った結果、膵癌症例の便中で、健常者よりも有意に多く存在する蛋白を同定しました。現在、これらの再現性について検証中です。
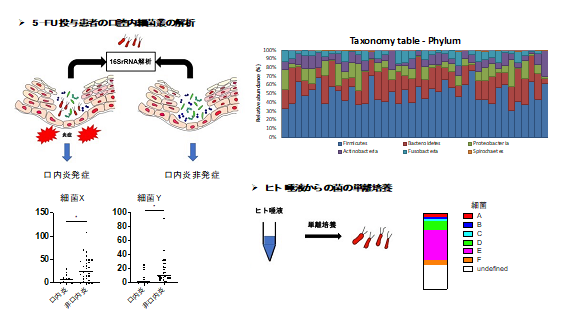
3. 5-FU口内炎に対する口腔内細菌叢の解析
担癌患者の5-FU投与前の唾液の口腔内細菌叢を解析した結果、口内炎非発症の症例で有意に多い菌を同定しました。それらの菌を唾液より単離培養して、口内炎の発症と細菌の関連について基礎研究を進めていく予定です。